
Tüm iLive içeriği tıbbi olarak incelenir veya mümkün olduğu kadar gerçek doğruluğu sağlamak için kontrol edilir.
Sıkı kaynak bulma kurallarımız var ve yalnızca saygın medya sitelerine, akademik araştırma kurumlarına ve mümkün olduğunda tıbbi olarak meslektaş gözden geçirme çalışmalarına bağlanıyoruz. Parantez içindeki sayıların ([1], [2], vb.) Bu çalışmalara tıklanabilir bağlantılar olduğunu unutmayın.
İçeriğimizin herhangi birinin yanlış, güncel değil veya başka türlü sorgulanabilir olduğunu düşünüyorsanız, lütfen onu seçin ve Ctrl + Enter tuşlarına basın.
DNA moleküllerine dayalı karmaşık bir sentetik aşı oluşturuldu
Makalenin tıp uzmanı
Son inceleme: 01.07.2025
Daha güvenli ve etkili aşılar üretmenin yollarını arayan Arizona Eyalet Üniversitesi Biyotasarım Enstitüsü'ndeki bilim insanları, tamamen yeni bir sentetik aşı türü geliştirmek için DNA nanoteknolojisi adı verilen umut verici bir alana yöneldi.
Nano Letters dergisinde yakın zamanda yayımlanan bir çalışmada, Biyomühendislik Enstitüsü'nden immünolog Yung Chang, ünlü DNA nanoteknolojisti Hao Yan da dahil olmak üzere meslektaşlarıyla bir araya gelerek, kendiliğinden birleşen, üç boyutlu DNA nanoyapılarına yerleştirilerek hedef bölgelere güvenli ve etkili bir şekilde ulaştırılabilen dünyanın ilk aşı kompleksini sentezledi.
"Hao, DNA'yı genetik materyal olarak değil, bir çalışma platformu olarak görmemizi önerdiğinde, bu yaklaşımı immünolojiye uygulama fikri aklıma geldi," diyor Biyomühendislik Enstitüsü'ndeki Yaşam Bilimleri Okulu'nda doçent ve Bulaşıcı Hastalıklar ve Aşılar Merkezi'nde araştırmacı olan Chang. "Bu, bize sentetik bir aşı oluşturmak için DNA taşıyıcılarını kullanma konusunda harika bir fırsat verecek."
"Büyük soru şuydu: Güvenli mi? Vücutta güvenli ve güçlü bir bağışıklık tepkisi tetikleyebilecek bir molekül grubu yaratmak istedik. Hao'nun ekibi son birkaç yıldır çeşitli DNA nanoyapıları tasarladığı için, bu yapılar için potansiyel tıbbi uygulamalar bulmak üzere iş birliği yapmaya başladık."
Arizonalı bilim insanlarının önerdiği yöntemin benzersizliği, antijen taşıyıcısının bir DNA molekülü olması.
Disiplinler arası araştırma ekibinde ayrıca Arizona Üniversitesi biyokimya yüksek lisans öğrencisi ve makalenin ilk yazarı Xiaowei Liu, profesör Yang Xu, biyokimya öğretim görevlisi Yan Liu, Biyolojik Bilimler Fakültesi öğrencisi Craig Clifford ve Çin'deki Sichuan Üniversitesi'nden yüksek lisans öğrencisi Tao Yu da yer aldı.
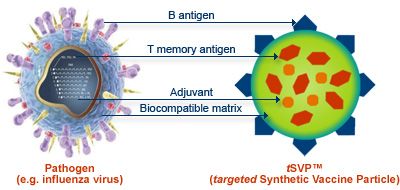
Chang, aşılamanın yaygın olarak benimsenmesinin halk sağlığının en önemli zaferlerinden birine yol açtığını belirtiyor. Aşı yaratma sanatı, bağışıklık sistemini uyaran proteinlerden virüs benzeri parçacıklar oluşturmak için genetik mühendisliğine dayanır. Bu parçacıklar yapı olarak gerçek virüslere benzerdir ancak hastalığa neden olan tehlikeli genetik bileşenler içermez.
Bir biyomoleküle iki veya üç boyutlu şekil verilmesine olanak tanıyan DNA nanoteknolojisinin önemli bir avantajı, vücuttaki doğal moleküllerin tipik işlevlerini yerine getirebilen moleküllerin çok hassas yöntemlerle oluşturulabilmesidir.
"Farklı boyutlarda ve şekillerde DNA nanoyapıları üzerinde deneyler yaptık ve vücudun nasıl tepki vereceğini görmek için bunlara biyomoleküller ekledik," diye açıklıyor Yang, Kimya ve Biyokimya Bölümü müdürü ve Biyomühendislik Enstitüsü'ndeki Tek Molekül Biyofiziği Merkezi'nde araştırmacı. Bilim insanlarının "biyomimikri" adını verdiği bir yaklaşımla, test ettikleri aşı kompleksleri doğal virüs parçacıklarının boyutunu ve şeklini yaklaşık olarak yansıtıyor.
Araştırmacılar, konseptlerinin uygulanabilirliğini göstermek için bağışıklık uyarıcı protein streptavidin (STV) ve bağışıklık güçlendirici ilaç CpG oligodeoksinükleotidini ayrı piramidal dallanmış DNA yapılarına bağladılar; bu da nihayetinde sentetik bir aşı kompleksi elde etmelerine olanak tanıyacaktı.
Ekibin ilk önce hedef hücrelerin nanoyapıları emebileceğini kanıtlaması gerekiyordu. Nanoyapıya ışık yayan bir etiket molekülü ekleyerek bilim insanları nanoyapının hücrede uygun yerini bulduğunu ve birkaç saat boyunca sabit kaldığını doğrulayabildiler; bu da bir bağışıklık tepkisini tetiklemeye yetecek kadar uzun bir süreydi.
Daha sonra, fareler üzerinde yapılan deneylerde bilim insanları, vücudun bağışıklık tepkisi zincirindeki ilk halkalar olan hücrelere aşı "yükünü" ulaştırmak, makrofajlar, dendritik hücreler ve B hücreleri gibi antijen sunan hücreler gibi farklı bileşenler arasındaki etkileşimleri koordine etmek üzerinde çalıştılar. Nanoyapılar hücreye girdikten sonra, hücre yüzeyinde "analiz edilir" ve "görüntülenir", böylece vücudun savunma tepkisini tetiklemede merkezi bir rol oynayan beyaz kan hücreleri olan T hücreleri tarafından tanınabilirler. T hücreleri ise B hücrelerinin yabancı antijenlere karşı antikor üretmesine yardımcı olur.
Tüm varyantları güvenilir şekilde test etmek için araştırmacılar hücrelere hem tam aşı kompleksini hem de sadece STV antijenini, ayrıca STV antijenini bir CpG güçlendirici ile karıştırılmış şekilde enjekte ettiler.
70 günlük bir sürenin ardından bilim insanları, tam aşı kompleksiyle aşılanan farelerin CpG/STV karışımıyla oluşturulandan 9 kat daha güçlü bir bağışıklık tepkisi gösterdiğini buldu. En belirgin tepki tetrahedral (piramidal) yapı tarafından başlatıldı. Ancak aşı kompleksine karşı bağışıklık tepkisi yalnızca spesifik (yani, deneyciler tarafından kullanılan spesifik bir antijene karşı vücudun tepkisi) ve etkili olarak değil, aynı zamanda hücrelere sokulan "boş" DNA'ya (biyomolekül taşımayan) karşı bir bağışıklık tepkisinin olmamasıyla doğrulanan güvenli olarak da kabul edildi.
"Çok memnun kaldık," diyor Chang. "Öngördüğümüz sonuçları görmek harikaydı. Biyolojide bu çok sık olmaz."
İlaç endüstrisinin geleceği hedeflenen ilaçlarda yatıyor
Şimdi ekip, bir DNA platformu kullanarak belirli bağışıklık hücrelerini bir tepkiyi tetikleyecek şekilde uyarmak için yeni bir yöntemin potansiyelini düşünüyor. Yeni teknoloji, birkaç aktif ilaçtan oluşan aşılar oluşturmak ve bağışıklık tepkisini düzenlemek için hedefleri değiştirmek için kullanılabilir.
Ayrıca yeni teknoloji, özellikle vücudun belirli bölgelerine uygulanan ve bu nedenle tehlikeli yan etkilere yol açmayan "hedefli" ilaçların üretimi olmak üzere, yeni hedefli tedavi yöntemlerinin geliştirilmesi potansiyeline sahiptir.
Son olarak, DNA alanı henüz emekleme aşamasında olmasına rağmen, Arizona araştırmacılarının bilimsel çalışmaları tıp, elektronik ve diğer alanlar için önemli pratik çıkarımlara sahiptir.
Chang ve Yang, aşı yöntemleri hakkında öğrenilecek ve optimize edilecek çok şey olduğunu kabul ediyorlar, ancak keşiflerinin değeri yadsınamaz. Chang, "Elimizde kavram kanıtıyla artık sınırsız sayıda antijen içeren sentetik aşılar üretebiliriz," diye sonuca varıyor.
Bu araştırmanın finansal desteği ABD Savunma Bakanlığı ve Ulusal Sağlık Enstitüleri tarafından sağlandı.
 [ 1 ], [ 2 ], [ 3 ], [ 4 ], [ 5 ], [ 6 ], [ 7 ], [ 8 ], [ 9 ]
[ 1 ], [ 2 ], [ 3 ], [ 4 ], [ 5 ], [ 6 ], [ 7 ], [ 8 ], [ 9 ]

