
Tüm iLive içeriği tıbbi olarak incelenir veya mümkün olduğu kadar gerçek doğruluğu sağlamak için kontrol edilir.
Sıkı kaynak bulma kurallarımız var ve yalnızca saygın medya sitelerine, akademik araştırma kurumlarına ve mümkün olduğunda tıbbi olarak meslektaş gözden geçirme çalışmalarına bağlanıyoruz. Parantez içindeki sayıların ([1], [2], vb.) Bu çalışmalara tıklanabilir bağlantılar olduğunu unutmayın.
İçeriğimizin herhangi birinin yanlış, güncel değil veya başka türlü sorgulanabilir olduğunu düşünüyorsanız, lütfen onu seçin ve Ctrl + Enter tuşlarına basın.
Restenoz
Makalenin tıp uzmanı
Son inceleme: 04.07.2025
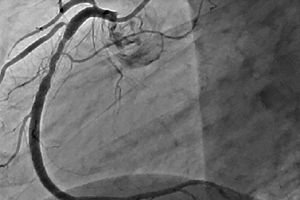
Restenoz, perkütan koroner müdahale bölgesinde %50 veya daha fazla tekrarlayan bir daralmanın gelişmesidir. Restenoz genellikle tekrarlayan angina ile birlikte görülür ve sıklıkla tekrarlanan müdahaleler gerektirir. PCI geliştikçe restenoz insidansı azaldı ve doğası da değişti.
Transluminal balon koroner anjiyoplasti (TBCA) sonrası restenoz
TBCA'dan sonra ilk 6 ayda restenoz oranı %30-40'tır. Gelişiminin ana mekanizması, özünde işlem sırasında balon tarafından genişletilen arter lümeninin elastik bir çöküşü olan damarın lokal negatif yeniden şekillenmesidir. Lokal trombüs oluşumu ve neointimal büyüme de göreceli bir rol oynar. TBCA'dan sonra restenoz için klinik (tip 2 diabetes mellitus, akut koroner sendrom (ACS), restenoz öyküsü), anjiyografik (LAD lezyonu, küçük damar çapı, kronik total oklüzyon (CTO), uzun lezyon, dejeneratif venöz bypass greftleri) ve prosedürel (büyük rezidüel stenoz, balon şişirme sonucu damar çapında küçük artış) risk faktörleri vardır. Restenoz durumunda genellikle tekrarlanan bir müdahale yapılır. Restenoz bölgesinde tekrarlanan TBCA'nın başarısı ilk işlemle karşılaştırılabilir. Ancak restenoz için yapılan her sonraki TBCA'da tekrarlayan restenoz riski önemli ölçüde artar. 3. denemeden sonra %50-53'e ulaşır. Ayrıca her tekrarlanan TBCA'da gelişen restenoz ilkinden daha belirgindir. İkinci TBCA'dan sonra restenoz için risk faktörleri, ilk restenozun erken ortaya çıkması (işlemden 60-90 gün sonra), LAD hasarı, multivesel hasarı, tip 2 diabetes mellitus, arteriyel hipertansiyon, kararsız angina ve ilk işlem sırasında çoklu balon şişirmeleridir. Yüksek restenoz sıklığı ve gelişim mekanizması göz önüne alındığında, teorik olarak TBCA'dan sonra negatif damar yeniden şekillenmesini ortadan kaldırması gereken koroner stentler klinik uygulamaya sokuldu.
Stentlemenin etkinliğini gösteren ilk çalışmalar 1993 yılında yayınlanan STRESS ve BENESTENT çalışmalarıdır. BENESTENT çalışması, çapı 3 mm'den büyük koroner arterlerde yeni teşhis edilmiş darlığı olan 516 hastayı içeriyordu ve randomize olarak iki gruba ayrıldı: geleneksel TBCA (n = 257) ve stent yerleştirilmiş TBCA (n = 259). 3 yıl sonra, anjiyografi sırasında restenoz oranı geleneksel TBCA grubunda %32, stentleme grubunda ise %22 idi. Restenoz oranındaki göreceli azalma %31 idi (p < 0,01). Stentleme grubunda ayrıca tekrarlanan miyokardiyal revaskülarizasyona daha az ihtiyaç duyuldu (geleneksel TBCA grubunda %10'a karşı %20,6; p < 0,01), bu da stentleme grubunda daha düşük angina tekrarlama oranıyla ilişkiliydi.
STRESS çalışmasına göre (n = 407), restenoz oranı stent grubunda (n ~ 205) geleneksel PTCA grubuna (n = 202) göre daha düşüktü - %31,6'ya karşı %42,1 (p < 0,01). PTCA bölgesinde restenoz durumunda geleneksel anjiyoplastiye göre stent kullanımının avantajı, restenozlu 383 hastanın stentleme veya tekrar perkütan transluminal koroner anjiyoplasti için randomize edildiği REST çalışmasında gösterilmiştir. Anjiyografik olarak tespit edilen tekrar restenoz, stentleme grubunda %18 daha düşüktü (%18'e karşı %5,32; p < 0,03). Klinik olarak anlamlı restenozun bir göstergesi olan tekrarlayan miyokardiyal revaskülarizasyon da stentleme uygulanan hasta grubunda önemli ölçüde daha az sıklıkta gerekti (%10'a karşı %27; p < 0,001). Böylece stent uygulamasının sadece natürel arterlerde değil, TBCA sonrası gelişen restenoz durumlarında da daha iyi sonuçlar verdiği kanıtlanmıştır.
Çıplak stent implantasyonundan sonra restenoz (BSI)
Açık koroner stentler, TBCA'ya kıyasla restenoz insidansını %30-40 oranında azaltmış olsa da, hastaların %17-32'sinde stent takıldıktan sonra bile stent içi restenoz gelişir ve tekrar revaskülarizasyon gerekir. Stent içi stenoz (ISS) gelişiminin mekanizması TBCA'dakinden farklıdır. Stent takıldıktan sonra restenoza ana katkı, stent implantasyon bölgesinde neredeyse hiç bulunmayan TBCA'daki gibi negatif yeniden şekillendirmeden ziyade neointima oluşumudur. Neointima, hücrelerle birlikte neointimayı oluşturan ekstraselüler matrisi üreten düz kas hücrelerinin göçü ve proliferasyonu ile oluşur. Ayrıca, stent bölgesinde trombüsün kalıcılığı diyabetli hastalarda da önemlidir.
Stent içi stenozun (ISS) ana sınıflandırması, lezyonun yaygınlığına ve ciddiyetine bağlı olarak dört tip içeren Mehran tarafından önerilen sınıflandırmadır: I tip ISS - lokal (< 10 mm uzunluğunda), II tip - difüz (> 10 mm uzunluğunda), III tip - proliferatif (> 10 mm ve stentin ötesine uzanan) ve IV tip - oklüzyona yol açan ISS. İlk tip, stent içindeki lokasyona bağlı olarak alt tiplere ayrılır: 1a - kıvrımda veya stentler arasında, 1b - marjinal, 1c - stentin içinde, 1d - multifokal.
VRS gelişimi için risk faktörleri, venöz bypass greftlerine yapılan müdahaleler, kronik oklüzyonlar, ostial lezyonlar, küçük damar çapı, rezidüel stenoz varlığı, VRS için stent takılması, küçük işlem sonrası damar çapı, LAD lezyonu, uzun stent uzunluğu, diyabet varlığı, bir lezyona birden fazla stent yerleştirilmesidir. Genetik faktörlerin, özellikle glikoprotein IIIa geninin polimorfizminin ve metilentetrahidrofolat redüktaz geninin mutasyonlarının - interlökin-1 kodlayan gen - etkisinin belirtileri vardır. Marjinal stent restenozunun gelişmesi durumunda, ana risk faktörü stentli segmentte belirgin bir aterosklerotik lezyondur.
Restenoz, perkütan koroner girişimden sonraki ilk 6-8 ayda baskın olarak ortaya çıkar. Çoğu hastada klinik semptomlar yaklaşık aynı zamanda gelişir. VRS genellikle tekrarlayan angina ile kendini gösterir. Kararsız angina daha az sıklıkla görülür (%11-41 vaka). AMI hastaların %1-6'sında gelişir. Bu nedenle, stent takıldıktan sonraki 1-6 aylık dönemde anginanın en yaygın nedeni, kural olarak tekrarlanan revaskülarizasyon gerektiren VRS gelişimidir. VRS'yi tedavi etmek için birkaç yöntem vardır. Konvansiyonel TBCA yapılabilir, bu da stent genişlemesinin daha da artmasına (damar çapındaki son artışa %56 katkı) ve neointimayı stent hücrelerinden iter (%44 katkı çapı). Ancak, çoğu vakada müdahale bölgesinde rezidüel restenoz görülür (ortalama %18). Ek olarak, TBCA'dan sonra, vakaların %11'inde tekrar revaskülarizasyon gerekir, daha sıklıkla multivassel hastalığı olan, düşük LVEF'li hastalarda, venöz bypass greftlerine müdahalelerde veya ilk VRS'nin erken ortaya çıkması durumunda. TBCA'dan sonra tekrar VRS geliştirme riski ayrıca lezyon türüne bağlıdır ve lokal restenoz durumunda %10'dan intra-stent oklüzyon durumunda %80'e kadar değişir. LES'in VRS bölgesine implantasyonu, tek başına TBCA'ya kıyasla tekrarlama riskini azaltmaz.
VRS'yi tedavi etmenin ikinci yöntemi, koroner arterin lümenine radyoaktif bir kaynak sokulmasını, düz kas hücrelerinin çoğalmasını önlemeyi ve buna bağlı olarak restenoz riskini azaltmayı içeren brakiterapidir. Ancak, ekipmanın yüksek maliyeti, prosedürün teknik karmaşıklığı ve geç stent trombozu (LT) insidansının artması, brakiterapiyi klinik kullanımdan neredeyse tamamen dışlamıştır.
VRS tedavisinde devrim niteliğinde bir an, ilaç salan stentlerin tanıtılmasıydı. Doğal arterlerdeki LES ile karşılaştırıldığında, VRS riskini %70-80 oranında azaltırlar. Zaten VRS gelişmiş hastalarda DES'in etkinliğine ilişkin ilk veriler, bu tür hastalarda SPG1 kullanıldığında, VRS tekrarlama sıklığının 6 ay sonra sadece %16 olduğu TAXUS III hasta kayıt defterinde elde edildi; bu, daha önce bahsedilen TBCA çalışmalarından daha düşüktür. LES restenozunda SES implantasyonundan sonra hastaları içeren TRUE kayıt defterinde, 9 ay sonra, çoğunlukla diabetes mellitus ve ACS'li hastaların %5'inden azında tekrar revaskülarizasyona ihtiyaç duyuldu. TROPICAL çalışması, restenoz bölgesinde DES implantasyonundan sonra hastalarda tekrarlayan restenoz sıklığını, brakiterapinin tedavi yöntemi olarak kullanıldığı GAMMA I ve GAMMA II çalışmalarının verileriyle karşılaştırdı. 6 ay sonra, tekrarlayan restenoz insidansı SPS grubunda anlamlı derecede daha düşüktü (%9,7'ye karşı %40,3; p < 0,0001). Stent trombozu ve miyokard enfarktüsü insidansının da SPS grubunda daha düşük olduğuna dikkat etmek önemlidir (TS 0,6'ya karşı %3,9; p = 0,08; MI - 1,8'e karşı %9,4; p = 0,004). SPS'nin brakiterapiye göre avantajı, NSC'de VRS geliştiren 384 hastanın brakiterapi veya SPS implantasyon gruplarına randomize edildiği randomize SISR çalışmasında doğrulandı. 9 ay sonra, tekrarlayan revaskülarizasyon ihtiyacı brakiterapiden sonra (%19,2) SPS implantasyon grubuna göre (%8,5) daha yüksekti ve bu da daha sık restenoz tekrarını yansıtıyordu. 3 yıl sonra, tekrarlayan stent restenozuna bağlı tekrar revaskülarizasyon ihtiyacını azaltma açısından SPS'nin avantajı devam etti (%19'a karşı %28,4). Gruplar arasında tromboz insidansında anlamlı bir fark yoktu.
SPS implantasyonu durumunda LES'li hastalarda tekrarlayan VRS gelişiminin ana faktörleri küçük damar çapı (< 2,5 mm), diffüz restenoz tipi ve hemodiyaliz gerektiren kronik böbrek yetmezliğinin varlığıdır. Randomize TAXUS V ISR çalışmasında SPS, brakiterapiye kıyasla tekrarlayan restenoz oranını %54 oranında azaltarak VRS tedavisinde de yüksek etkinlik göstermiştir.
TBCA'nın VRS ve DES implantasyonu için etkinliğini karşılaştıran randomize çalışmalar da yürütüldü. Randomize RIBS-II çalışmasında, 9 ay sonra, DES implantasyonundan sonra tekrarlayan restenoz, TBCA'dan sonra olduğundan %72 daha az yaygındı; bu, tekrarlayan revaskülarizasyon ihtiyacını %30'dan %11'e düşürdü. ISAR DESIRE çalışması, TBCA'nın VRS için etkinliğini SPP veya SPS implantasyonuyla karşılaştırdı. 6 ay sonra, her iki DES'in de tekrarlayan restenozu önlemede TBCA'dan daha etkili olduğu ortaya çıktı (insidansı TBCA ile %44,6, SPS grubunda %14,3 ve SPS grubunda %21,7 idi), bu da tekrarlayan revaskülarizasyon ihtiyacını azalttı. SPP ve SPS'nin doğrudan karşılaştırılmasında, SPS'nin tekrarlayan revaskülarizasyon ihtiyacını SPP'den önemli ölçüde daha etkili bir şekilde azalttığı bulundu (%8'e karşı %19). Bu nedenle DES implantasyonu, hem TBCA hem de brakiterapiye kıyasla tekrarlayan LES VRS insidansını azaltır, bu da tekrarlayan PCI sayısını azaltır ve dolayısıyla bu tür hastalarda DES implantasyonunu tercih edilen prosedür haline getirir.
İlaç salan stent (DES) implantasyonundan sonra restenoz
DES kullanıldığında LES'e kıyasla stent içi stenoz insidansında %70-80'lik bir azalmaya rağmen, stentlemenin bu iatrojenik sonucunun gelişimini tamamen dışlayamadılar. Genel insidansı ortalama olarak %10'dan az kalmaktadır. Restenoz insidansındaki niceliksel azalmaya ek olarak, oluşan restenoz tipini de önemli ölçüde değiştirdiler. Bu nedenle, DES implantasyonundan sonra restenoz genellikle fokaldir. Klinik olarak, LES durumunda olduğu gibi, en sık stabil angina nüksü olarak kendini gösterir (%77), daha az sıklıkla (%8) asemptomatiktir. Vakaların %5'inde kararsız angina olarak kendini gösterir ve %10'unda ilk semptomu Q dalgası olmayan miyokard enfarktüsü olur. DES restenozunun gelişimindeki ana faktörler tip 2 diabetes mellitus, küçük damar çapı ve lezyonun yaygınlığıdır. Bu tür hastaların yönetimi için net öneriler yoktur. Alternatif seçenekler arasında bir DES'in (aynı tipte veya farklı bir tipte) yeniden implantasyonu, TBCA veya brakiterapi yer alır. İkinci bir DES ile tekrar restenoz oranının ortalaması %24'tür ve aynı tipte veya farklı bir DES implante edilmesinin bir önemi yoktur.


 [
[